O-Acetylserine (PAMDB000473)
| Record Information | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Version | 1.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Update Date | 1/22/2018 12:54:54 PM | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metabolite ID | PAMDB000473 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
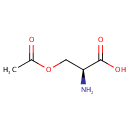
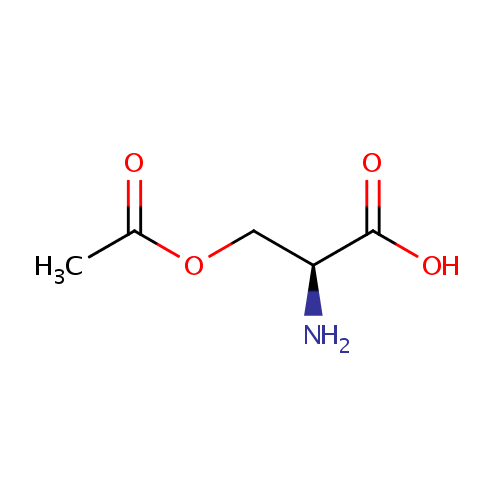
| Name: | O-Acetylserine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description: | O-Acetylserine is an intermediate in the biosynthesis of the common amino acid cysteine in bacteria and plants. O-Acetylserine is biosynthesized by acetylation of the serine by the enzyme serine transacetylase. The enzyme O-acetylserine (thiol)-lyase, using sulfide sources, converts this ester into cysteine, releaseing acetate. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyms: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Formula: | C5H9NO4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Average Molecular Weight: | 147.1293 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Monoisotopic Molecular Weight: | 147.053157781 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI Key: | VZXPDPZARILFQX-BYPYZUCNSA-N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI: | InChI=1S/C5H9NO4/c1-3(7)10-2-4(6)5(8)9/h4H,2,6H2,1H3,(H,8,9)/t4-/m0/s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS number: | 5147-00-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC Name: | (2S)-3-(acetyloxy)-2-aminopropanoic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Traditional IUPAC Name: | O-acetyl-L-serine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES: | CC(=O)OC[C@H](N)C(O)=O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Taxonomy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taxonomy Description | This compound belongs to the class of organic compounds known as l-alpha-amino acids. These are alpha amino acids which have the L-configuration of the alpha-carbon atom. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kingdom | Organic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Super Class | Organic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Class | Carboxylic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sub Class | Amino acids, peptides, and analogues | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direct Parent | L-alpha-amino acids | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alternative Parents | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Substituents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molecular Framework | Aliphatic acyclic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Descriptors |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| State: | Solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Charge: | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Experimental Properties: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicted Properties |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Biological Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cellular Locations: | Cytoplasm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reactions: | O-Acetylserine + Hydrogen sulfide <> Acetic acid + L-Cysteine + Hydrogen ion Acetyl-CoA + L-Serine <> O-Acetylserine + Coenzyme A O-Acetylserine + Hydrogen sulfide <> L-Cysteine + Acetic acid O-Acetylserine + Thiosulfate <> Cysteine-S-sulfate + Acetic acid O-Acetylserine + Hydrogen selenide <> Selenocysteine + Acetic acid O-Acetylserine + Thiosulfate + Thioredoxin + Hydrogen ion <> L-Cysteine + Sulfite + Thioredoxin disulfide + Acetic acid L-Serine + Acetyl-CoA + L-Serine > Coenzyme A + O-Acetylserine O-Acetylserine > Hydrogen ion + Acetic acid + L-Cysteine O-Acetylserine + Thiosulfate + Thiosulfate > Cysteine-S-sulfate + Acetic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pathways: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synthesis Reference: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Material Safety Data Sheet (MSDS) | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Links | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Links: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Enzymes
- General function:
- Involved in transferase activity
- Specific function:
- Acetyl-CoA + L-serine = CoA + O-acetyl-L- serine
- Gene Name:
- cysE
- Locus Tag:
- PA3816
- Molecular weight:
- 27.9 kDa
Reactions
| Acetyl-CoA + L-serine = CoA + O-acetyl-L-serine. |
- General function:
- Involved in cysteine biosynthetic process from serine
- Specific function:
- O(3)-acetyl-L-serine + H(2)S = L-cysteine + acetate
- Gene Name:
- cysK
- Locus Tag:
- PA2709
- Molecular weight:
- 34.3 kDa
Reactions
| O(3)-acetyl-L-serine + H(2)S = L-cysteine + acetate. |
| 3-chloro-L-alanine + thioglycolate = S-carboxymethyl-L-cysteine + chloride. |
- General function:
- Involved in cysteine biosynthetic process from serine
- Specific function:
- Two cysteine synthase enzymes are found. Both catalyze the same reaction. Cysteine synthase B can also use thiosulfate in place of sulfide to give cysteine thiosulfonate as a product
- Gene Name:
- cysM
- Locus Tag:
- PA0932
- Molecular weight:
- 32.4 kDa
Reactions
| O(3)-acetyl-L-serine + H(2)S = L-cysteine + acetate. |