beta-Alanine (PAMDB000019)
| Record Information | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Version | 1.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Update Date | 1/22/2018 12:54:54 PM | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metabolite ID | PAMDB000019 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
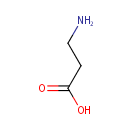
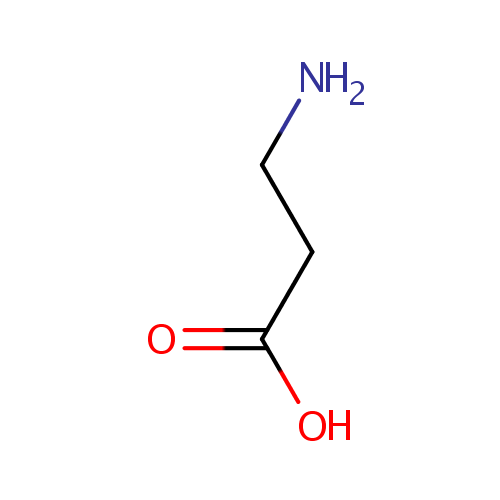
| Name: | beta-Alanine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description: | Beta-alanine is the only naturally occurring beta-amino acid. However, it is not used in the biosynthesis of any major proteins or enzymes. It is formed in vivo by the degradation of dihydrouracil and carnosine. It is a component of pantothenic acid (vitamin B5), which itself is a component of coenzyme A. Under normal conditions, beta-alanine is metabolized into acetic acid. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyms: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Formula: | C3H7NO2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Average Molecular Weight: | 89.0932 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Monoisotopic Molecular Weight: | 89.047678473 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI Key: | UCMIRNVEIXFBKS-UHFFFAOYSA-N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI: | InChI=1S/C3H7NO2/c4-2-1-3(5)6/h1-2,4H2,(H,5,6) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS number: | 107-95-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC Name: | 3-aminopropanoic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Traditional IUPAC Name: | β alanine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES: | NCCC(O)=O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Taxonomy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taxonomy Description | This compound belongs to the class of organic compounds known as beta amino acids and derivatives. These are amino acids having a (-NH2) group attached to the beta carbon atom. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kingdom | Organic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Super Class | Organic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Class | Carboxylic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sub Class | Amino acids, peptides, and analogues | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direct Parent | Beta amino acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alternative Parents | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Substituents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molecular Framework | Aliphatic acyclic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Descriptors |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| State: | Solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Charge: | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point: | 200 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Experimental Properties: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicted Properties |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Biological Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cellular Locations: | Cytoplasm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reactions: | L-Aspartic acid + Hydrogen ion <> beta-Alanine + Carbon dioxide beta-Alanine + Adenosine triphosphate + (R)-Pantoate <> Adenosine monophosphate + Hydrogen ion + Pantothenic acid + Pyrophosphate L-Aspartic acid <> beta-Alanine + Carbon dioxide beta-Alanine + alpha-Ketoglutarate <> Malonic semialdehyde + L-Glutamate Adenosine triphosphate + (R)-Pantoate + beta-Alanine <> Adenosine monophosphate + Pyrophosphate + Pantothenic acid L-Aspartic acid + Hydrogen ion + L-Aspartic acid Carbon dioxide + beta-Alanine beta-Alanine + Adenosine triphosphate + (R)-pantoate + (R)-Pantoate > Adenosine monophosphate + Pyrophosphate + Hydrogen ion + Pantothenic acid + Pantothenic acid beta-Alanine + Adenosine triphosphate > Adenosine monophosphate + Pyrophosphate + Hydrogen ion | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pathways: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synthesis Reference: | Buc, Saul R.; Ford, Jared H.; Wise, E. C. Improved synthesis of b-alanine. Journal of the American Chemical Society (1945), 67 92-4. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Material Safety Data Sheet (MSDS) | Download (PDF) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Links | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Links: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Enzymes
- General function:
- Involved in aspartate 1-decarboxylase activity
- Specific function:
- Catalyzes the pyruvoyl-dependent decarboxylation of aspartate to produce beta-alanine
- Gene Name:
- panD
- Locus Tag:
- PA4731
- Molecular weight:
- 13.9 kDa
Reactions
| L-aspartate = beta-alanine + CO(2). |
- General function:
- Involved in 4-aminobutyrate transaminase activity
- Specific function:
- 4-aminobutanoate + 2-oxoglutarate = succinate semialdehyde + L-glutamate
- Gene Name:
- gabT
- Locus Tag:
- PA0266
- Molecular weight:
- 45.2 kDa
Reactions
| 4-aminobutanoate + 2-oxoglutarate = succinate semialdehyde + L-glutamate. |
| (S)-3-amino-2-methylpropanoate + 2-oxoglutarate = 2-methyl-3-oxopropanoate + L-glutamate. |
- General function:
- Involved in catalytic activity
- Specific function:
- Catalyzes the condensation of pantoate with beta-alanine in an ATP-dependent reaction via a pantoyl-adenylate intermediate
- Gene Name:
- panC
- Locus Tag:
- PA4730
- Molecular weight:
- 30.8 kDa
Reactions
| ATP + (R)-pantoate + beta-alanine = AMP + diphosphate + (R)-pantothenate. |